上海巴斯德所发现NCoR1在未成熟T细胞发育选择过程起重要质量控制作用
10月16日,国际学术期刊Nature Communications在线发表了中科院上海巴斯德研究所冷启彬研究组的最新研究成果“NCoR1 restrains thymic negative selection by repressing Bim expression to spare thymocytes undergoing positive selection”。该研究揭示了NCoR1(nuclear receptor co-repressor 1)在胸腺T细胞的关键发育过程起质量控制调节作用。
T细胞需要在胸腺组织中发育为成熟的T细胞才能迁移至外周组织,其中最重要的是阳性选择和阴性选择过程。T细胞发育过程中,机体为了防止T细胞识别机体自身蛋白(抗原)避免发生自身免疫病将与自身抗原有较高亲和力的未成熟T细胞清除的过程即为阴性选择;而与自身抗原有适中亲和力的未成熟T细胞获得存活下来的过程称之为阳性选择。获得阴性选择的细胞最终发育为成熟的单阳性T细胞,并迁移至外周组织中在抗击病毒和细菌等感染性疾病方面发挥关键作用。然而保证未成熟的T细胞正常进行阳性选择、从而幸免于阴性选择的转录机制仍然不清楚,因此对T细胞发育的机制研究有待深入探究。
NCoR1 即核受体辅抑制因子1 (Nuclear receptor co-repressor 1),在肿瘤发生、脂肪代谢及肌肉活动中都具有很重要的调节作用。关于NCoR1对T细胞的调控作用的研究报道不多,仅2000年Jepsen等人的研究结果表明,NCoR1在T细胞的早期CD4-CD8-双阴性(DN)T细胞发育中起重要作用。冷启彬课题组建立了T细胞特异性缺失NCoR1的小鼠品系,发现NCoR1缺失并不导致胸腺细胞停止在DN T细胞阶段而是阻碍了CD4+CD8+双阳性(DP)阶段到CD4+或者CD8+单阳性(SP)阶段的晚期分化过程,进而导致外周成熟T细胞也相应的减少。深入研究发现,单阳性T细胞的减少是因为正在进行阳性选择的未成熟T细胞被阴性选择而发生了凋亡导致。进一步的分子生物学和生物信息学分析研究发现,NCoR1缺失导致促凋亡蛋白Bim表达水平显著提高。在野生型小鼠胸腺未成熟的T细胞中,NCoR1蛋白可以结合到Bim启动子区域通过表观遗传机制抑制Bim基因的表达,而且高强度的T细胞激活信号促进NCoR1蛋白与Bim启动子解离、促进Bim蛋白的表达进而细胞凋亡。比较研究NCoR1和Bim双基因敲除及其单基因敲除小鼠还发现,Bim的缺失的确可以拯救因NCoR1缺失而导致的T细胞发育缺陷。该研究阐述了在T细胞发育过程中上游T细胞信号的强弱水平最终通过调控Bim基因转录水平决定未成熟T细胞的命运,而NCoR1通过对Bim基因的转录抑制作用在平衡未成熟T细胞的阳性选择和阴性选择的阈值中起关键作用。
该研究是在冷启彬教授和Ronald M Evans教授的共同指导下,由上海巴斯德所的研究生王建荣、张娜与美国salk生物研究机构的何南海博士等人完成。该研究获得了国家自然科学基金、法国道达尔基金以及美国NIH基金等的经费支持。
文章链接: https://www.nature.com/articles/s41467-017-00931-8
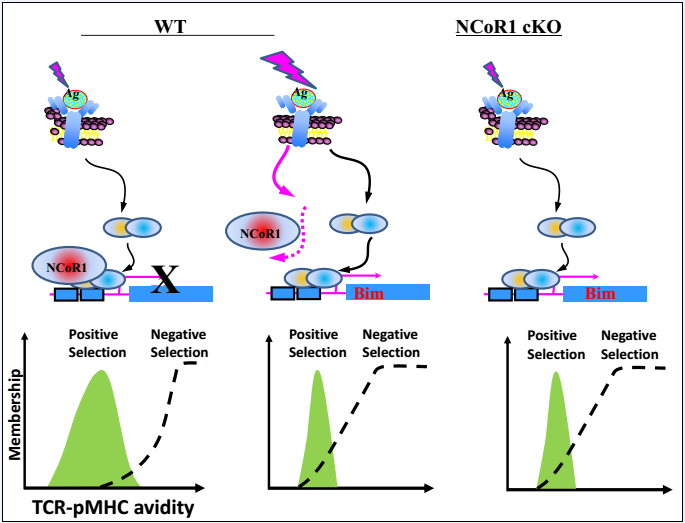
文章配图
附件下载: